Le PCV2 est-il un nouveau virus dans l'élevage porcin ?
On a connaissance de l'existence du PCV2 depuis 1998 suite à la recherche de la cause d'épisodes cliniques décrits à partir de 1991. Ces épisodes concernaient principalement des retards de croissance et une augmentation de mortalité chez des porcs en fin de PS et en première partie d'engraissement, nommant cet état pathologique la maladie d'amaigrissement du porcelet (aujourd'hui, on a proposé de l'appeler maladie systémique associée au PCV2, MS-PCV2). Les principaux épisodes épidémiques ont eu lieu en Europe et en Asie entre 1998 et 2004 tandis que sur le continent américain ils ont eu lieu entre 2004 et 2007. Cependant, on a eu une constance grâce à des études rétrospectives de l'existence d'animaux infectés par le PCV2 au moins depuis 1962 et d'animaux avec MS-PCV2 depuis au moins 1985.

LE PCV 2 est-il un virus fréquent ?
Depuis la première description du PCV2 en 1998, on a mis en évidence la présence du virus dans tous les pays dans lesquels il a été recherché, démontrant qu'il s'agit d'un virus ubiquiste au niveau mondial. De la même manière, pratiquement 100 % des élevages commerciaux sont infectés par le PCV2 et presque la totalité des porcs sont séropositifs au PCV2 en fin d'engraissement. On a aussi montré la répartition mondiale De MS-PCV2 comme l'indique la figure 1.
Figure 1 : Pays dans lesquels on a diagnostiqué MS-PVC2 (en jaune).
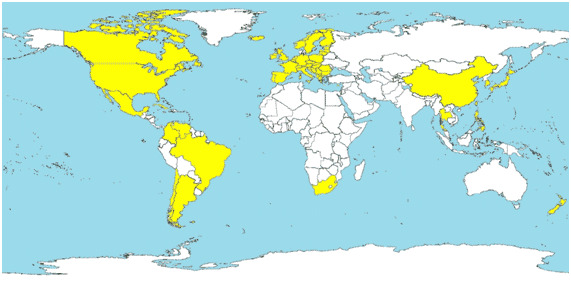
Comment se transmet le PCV2?
Les animaux infectés par le PCV2 éliminent le virus par toutes les voies d'excrétion examinées ; il est détecté dans la cavité nasale, la sécrétion oro-amygdalienne, la sécrétion bronchiale, la salive, la sécrétion oculaire, les fèces, l'urine, le lait et la semence. La voie de transmission principale est oronasale, bien que le PCV2 ait une forte résistance dans l'environnement et que la transmission aérogène soit possible.
Dans un élevage, les animaux reproducteurs sont ceux qui "maintiennent" l'infection et qui la transmettent aux porcelets habituellement par voie horizontale pendant l'allaitement. Cependant, on a aussi décrit la transmission verticale chez ce groupe d'animaux.
L'information concernant la dynamique d'infection par le PCV2 dans un élevage peut être consultée dans l'article précédent "Effet de la virémie par le circovirus porcin de type 2 (PCV2) sur les paramètres de production".
La capacité potentielle d'infection de la semence a été uniquement démontrée dans des conditions expérimentales après l'inoculation intrapéritonéale de la semence infectée sur des porcelets ou en reproduisant la maladie de la reproduction associée au PCV2 après avoir inséminé des truies avec de la semence expérimentalement infectée. Jusqu'à ce jour on n'a pas décrit de transmission de l’infection à la truie ni aux fœtus après l'insémination artificielle par de la semence naturellement infectée. Donc, ces expériences montrent que l'infection par la semence n'est pas un fait fréquent ni simple puisque la charge virale habituelle sur le terrain n'est peut-être pas suffisamment élevée pour être infectante.
A quoi est dû son comportement pathogénique relativement récent ?
Il n'existe pas d'explication simple au fait que le PCV2, virus ubiquiste, s'associe à l'apparition épidémique d'une maladie de forme relativement subite et globale. Il est très possible qu'il existe différents aspects relatifs à la production porcine et au commerce international qui peuvent partiellement l'expliquer. Cependant, on sait actuellement que ce changement de forme clinique, de sporadique à épidémique, est associé à un changement dans la prévalence de génotype PCV2a vers le PCV2b. Un exemple de cette situation est montré à partir des données provenant d'Espagne sur la figure 2. D'un autre côté, il existe quelques études qui montrent une plus grande probabilité de reproduire la maladie en utilisant des inoculums de PCV2b que de PCV2a.
Figure 2. Fréquence de détection de PCV2a et PCV2b en Espagne (adapté de Cortey et al., 2011 Vet J).
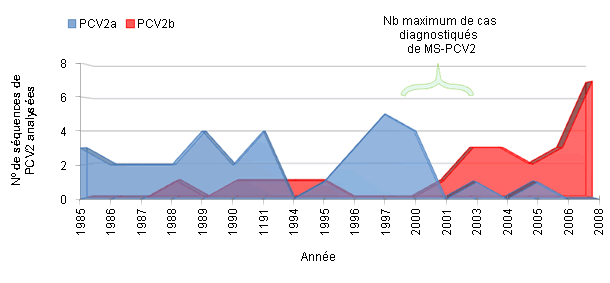 Une donnée curieuse dans ce sens est l'existence de protection croisée que confère le génotype "a" face au “b”, étant donné que les vaccins commerciaux existants sont aujourd'hui basés sur un virus du premier génotype.
Une donnée curieuse dans ce sens est l'existence de protection croisée que confère le génotype "a" face au “b”, étant donné que les vaccins commerciaux existants sont aujourd'hui basés sur un virus du premier génotype.
Quels facteurs peuvent avoir de l'influence que l'expression des PCVDs (1) ?
Le tableau clinique que les animaux peuvent développer dépend de nombreux facteurs comme leur âge, leur protection immunitaire passive ou active, la pression d'infection, la charge virale individuelle, la voie de transmission, leur situation physiologique (moment de gestation), en plus de la présence d'infections concomitantes et de facteurs environnementaux. Ainsi, de nombreuses études épidémiologiques ont décrit une série de facteurs de risque associés au développement du MS-PCV2 qui dans le tableau 1 (il s'agit d'un récapitulatif de résultats obtenus dans différentes études, en général avec un objectif exploratoire, où parfois l'association biologique n'est à priori pas évidente dans certains des cas car il s’agit de cas complexes)
Tableau 1 : Facteurs en relation avec l'augmentation et la diminution du risque de développer MS-PCV2
| Facteurs qui augmentent le risque de développer MS-PCV2 | Facteurs qui diminuent le risque de développer MS-PCV2 |
PCV2 :
Individu:
Installations:
Conduite:
Co-infections/vaccinations:
|
Installations:
Conduite:
Traitements/Vaccinations:
Biosécurité:
|
1PCVDs: maladies associée au circovirus porcin de type 2 (initiales provenant de l'anglais Porcine Circovirus Diseases).







