Actuellement, plusieurs techniques de laboratoire avancées sont utilisées pour évaluer la réponse immunitaire cellulaire chez le porc, soit en utilisant des cellules immunitaires du sang (cellules mononucléées du sang périphérique, PBMC), soit des cellules immunitaires dérivées d'organes périphériques tels que le thymus, les ganglions lymphatiques, la rate, l'intestin, le poumon et la moelle osseuse. Ces techniques se sont beaucoup améliorées en médecine vétérinaire et peuvent maintenant être utilisées en recherche expérimentale ou sur le terrain. La cytométrie en flux est également utilisée en oncologie pour petits animaux.
L’une des techniques les plus utilisées est l’analyse ELISPOT de l’IFN-γ, qui permet de quantifier avec une grande sensibilité le nombre de cellules sécrétrices d’IFN-γ par leur stimulation avec un antigène viral (par exemple, SDRPv, PCV2, ADV) ou des antigènes. mycoplasmiques / bactériens (par exemple, Mycoplasma hyopneumoniae, Escherichia coli).

Les PBMC sont isolées à partir de sang total d'animaux ayant été en contact avec l'agent pathogène, par des vaccinations antérieures et / ou des infections naturelles. Les lymphocytes T sont quantifiés en les faisant réagir avec un antigène du même agent pathogène, ou l'agent pathogène tout entier lui-même (par exemple, le virus entier). ).
Ce test peut fournir des informations pertinentes sur l'état d'activation du système immunitaire de l'animal. En fait, l'induction spécifique par le virus ou les bactéries sur les cellules mémoire et les cellules effectrices T est détectée par la sécrétion d'IFN-γ au niveau cellulaire, visualisée dans 96 puits.
En utilisant l'ELISPOT, il est possible de surveiller la réactivité immunitaire au fil du temps en comparant les formes de vaccination (par exemple, intramusculaire vs intradermique sans aiguille; les programmes de vaccination peuvent également être comparés ou des infections par des agents pathogènes émergents peuvent être réalisées afin d'évaluer la réponse des animaux infectés et l'efficacité de nouveaux vaccins en termes de protection et de protection croisée.
La réponse immunitaire cellulaire est évaluée en comptant les points produits par la sécrétion d'IFN-γ par chaque cellule et elle est généralement exprimée en nombre de cellules sécrétant l'IFN-γ par million de cellules analysées. Si l'échantillon est positif, cela signifie que l'animal a été exposé à l'antigène viral ou bactérien sur le terrain et qu'il a donc développé une immunité avec des lymphocytes T mémoire qui confère un degré de protection contre une exposition ultérieure au même agent pathogène et / ou une protection croisée contre les variantes de l'agent pathogène.
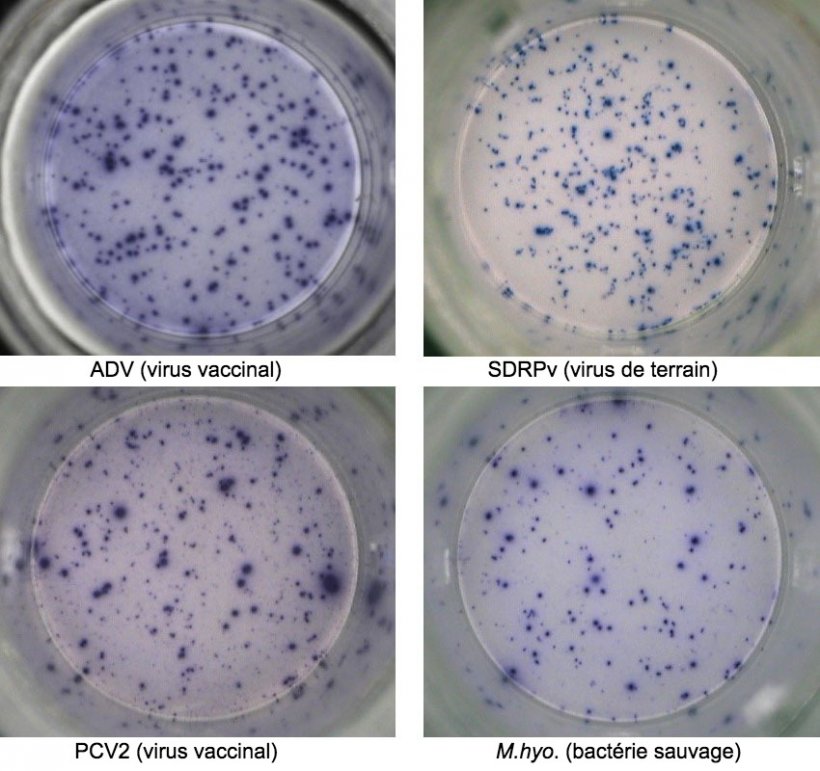
Figure 1. Réponse ELISPOT IFN-γ antigène-spécifique dans des PBMC contre des agents pathogènes porcins. ADV: virus de la maladie d'Aujeszky; SDRPv: virus du syndrome dysgénésique et respiratoire porcin; PCV2: circovirus porcin de type 2; M.hyo.: Mycoplasma hyopneumoniae. Chaque point est dû à la sécrétion d'IFN-γ par des lymphocytes T mémoire / effecteurs réactivés. L'agent pathogène utilisé pour réactiver les cellules dans les puits est indiqué entre parenthèses.
La cytométrie en flux est une technique sensible et spécifique qui permet d’identifier (immunophénotypage) et de quantifier les sous-populations de cellules immunitaires dans le sang périphérique (PBMC) ou les cellules isolées de tissus ou d’organes immunitaires qui sont colorés avec des anticorps conjugués au fluorochrome qui réagissent avec les principaux marqueurs immunitaires intracellulaires ou de surface.
Par conséquent, les modifications de ces sous-groupes peuvent être observées et surveillées au cours de traitements expérimentaux spécifiques ou de traitements sur le terrain, tels que les vaccinations ou l'administration d'immunostimulants ou d'autres médicaments ou les infections naturelles ou expérimentales. Normalement, les marqueurs les plus couramment utilisés pour la cytométrie en flux sont les molécules CD (cluster de différenciation) exprimées à la surface des cellules immunitaires, au moyen desquelles il est possible d'identifier plusieurs sous-groupes de monocytes (par exemple, CD172, CD14, CD16, CD163) et de lymphocytes (CD3, CD4, CD8, CD27, CD1, CD2, CD16, CD14, CD25, CD79).
L'état d'activation de ces cellules peut également être déterminé par coloration intracellulaire de molécules liées à l'activation et à la sécrétion de molécules telles que les cytokines pro-inflammatoires (par exemple, IL-1, TNF-α, IL-6), les immunocytokines (par exemple, IL-2, IFN-γ, IL-10) et les facteurs d’expression (par exemple, FoxP3).
De cette façon, après une infection et en utilisant plusieurs colorations, des sous-ensembles immunitaires polyfonctionnels capables de produire plusieurs cytokines simultanément peuvent être identifiés et étudiés. Celles-ci semblent être les cellules pertinentes capables de réguler et d'éliminer les agents pathogènes et d'offrir une protection contre eux.
![Figure 2. Exemples de cytométrie en flux permettant de détecter les phénotypes de cellules immunitaires quantifiés en pourcentage de valeurs absolues [nombre de cellules / ml de sang] chez des PBMC de porc:
a-c) Sous-populations de lymphocytes T: CD3 + CD4 + CD8- = lymphocytes T helper (Th) CD3 + CD4 + CD8 + = lymphocytes T mémoire CD3 + CD4 + CD8 + = lymphocytes T cytotoxiques (CTL)
d-e) sous-populations de monocytes pro-inflammatoires: CD172 + CD14 + CD16 + CD172 + CD16 + CD163 + CD172 + CD172 + CD143 + CD163 +
f-g) CD4 + CD25 + FoxP3 + = lymphocytes T régulateurs (Tregs).](https://www.3trois3.com/3tres3_common/art/3trois3/13376/cytometrie-en-flux_140907.jpg?w=820&q=1&ts=1653979446)
Figure 2. Exemples de cytométrie en flux permettant de détecter les phénotypes de cellules immunitaires quantifiés en pourcentage de valeurs absolues [nombre de cellules / ml de sang] chez des PBMC de porc:
a-c) Sous-populations de lymphocytes T: CD3 + CD4 + CD8- = lymphocytes T helper (Th) CD3 + CD4 + CD8 + = lymphocytes T mémoire CD3 + CD4 + CD8 + = lymphocytes T cytotoxiques (CTL)
d-e) sous-populations de monocytes pro-inflammatoires: CD172 + CD14 + CD16 + CD172 + CD16 + CD163 + CD172 + CD172 + CD143 + CD163 +
f-g) CD4 + CD25 + FoxP3 + = lymphocytes T régulateurs (Tregs).
La lymphoprolifération après une stimulation in vitro avec des activateurs mitogènes polyclonaux (non spécifiques) et monoclonaux (spécifiques, par exemple, pour les virus ou les bactéries) peut être un moyen facile d’évaluer la réactivité des lymphocytes T lorsque l’animal est soumis à des traitements susceptibles d’altérer la réponse aux mitogènes ou aux antigènes pathogènes qui activent la prolifération et induisent le passage de cellules quiescentes à des cellules proliférantes activées (c'est-à-dire des lymphoblastes).
La lymphoprolifération peut être évaluée par un test MTT (incorporation et changement de couleur d'un réactif par des cellules en prolifération) mais également par cytométrie en flux, quantification des lymphoblastes (grandes cellules) et / ou par incorporation de réactifs de prolifération fluorescents après stimulation in vitro pendant 2-5 jours.
La technologie des tétramères a été utilisée chez les porcs pour la quantification par cytométrie en flux de lymphocytes T cytolytiques / cytotoxiques de mémoire antigène-spécifiques CD8 + y et, plus récemment, pour la quantification des lymphocytes B mémoire antigène-spécifiques.

Elle est basée sur l’utilisation de macromolécules fluorescentes chargées d’antigènes exposés à une population mixte de cellules immunitaires afin d’interagir avec les cellules B et T, qui reconnaissent sélectivement l’antigène et sont probablement responsables de l’efficacité de la réponse cellulaire et de l'élimination / réduction de l'agent pathogène dans le corps de l'animal. C'est une méthode très spécifique et sensible capable de détecter de petites quantités de cellules mémoire B et T. Par exemple, elle a été développée pour détecter les lymphocytes T cytotoxiques CD8 + spécifiques du virus de la fièvre aphteuse (FMDv) et de la grippe porcine (SIV) et les lymphocytes B à mémoire spécifiques du SDRPv.
Les tests de cytotoxicité utilisent des lymphocytes T effecteurs cytolytiques / cytotoxiques (E) préalablement isolés qui sont incubés pendant 3-4 jours dans 96 puits avec des cellules cibles (T) à différents rapports (E / T); l'efficacité de la cytolyse fournit des informations sur le potentiel immunitaire des lymphocytes T effecteurs contre les cellules cibles potentiellement infectées in vivo.





